近日,我院彭涛课题组在《德国应用化学》(Angewandte Chemie International Edition)发表通讯论文,报道了首例基于甲醛化学反应活性的新型基因编码甲醛荧光探针和生物发光探针。
众所周知,甲醛是一种广泛用于工业生产的基本化学原料,也是一种常见的环境污染物和致癌物。但少为人知的是,哺乳动物和人体内的一系列正常生命活动也能产生内源性甲醛。在生理条件下,生物体内源甲醛的浓度维持在一个稳定的水平,作为一碳代谢中间产物用于制造重要的细胞结构单元并作为信号分子参与正常的生理过程。然而过量的甲醛却能引起蛋白质和核酸形成分子交联,影响基因的正常表达以及蛋白质的结构和功能。因此,内源甲醛浓度的异常增高已经与多种疾病的病理过程联系在一起,包括癌症和阿尔茨海默症等。为了深入研究甲醛在生理和病理条件下的确切作用和机制,并开发基于内源甲醛的新诊断和治疗方法,发展能用于生物体系中进行甲醛检测的探针至关重要。由于荧光探针和生物发光探针具有快捷、高灵敏度、高选择性、非侵入性以及时空成像能力等优点,科学家们开发了多种检测甲醛的小分子荧光探针和生物发光探针。相比于小分子探针,基于蛋白质的可基因编码的荧光探针和生物发光探针以DNA的形式引入活细胞或生物体内,具有独特的优势,如优越的细胞滞留能力,细胞特异和亚细胞器特异靶向性,以及稳定持久的标记等。然而,基因编码的甲醛荧光探针和生物发光探针目前还鲜有报道。
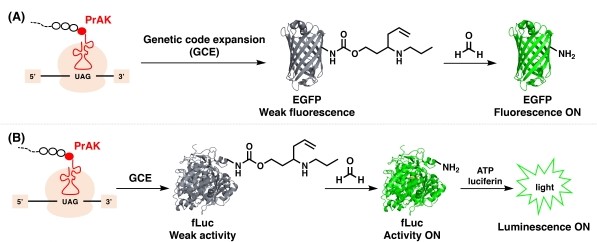
彭涛课题组巧妙地整合了甲醛的化学反应活性、化学生物学前沿的基因密码子扩展技术以及蛋白质活性调控,成功开发了新型基因编码的甲醛荧光探针和生物发光探针。研究人员设计合成了具有高烯丙基胺侧链的赖氨酸衍生物PrAK,能选择性地与甲醛进行2-氮杂-Cope重排反应,并通过水解和消除生成赖氨酸。利用基因密码子扩展技术,研究人员分别将非天然氨基酸PrAK位点特异地插入增强绿色荧光蛋白(EGFP)和萤火虫荧光素酶(fLuc)的关键赖氨酸残基上,构建基因编码的甲醛荧光探针和生物发光探针。与甲醛反应之前,由于关键赖氨酸位点缺失,引入PrAK的EGFP和fLuc探针分别表现出微弱的荧光和生物发光酶活性;当甲醛存在时,其与PrAK残基发生选择性2-氮杂-Cope重排反应生成赖氨酸,导致EGFP和fLuc探针的荧光和生物发光酶活性显著增强,从而实现甲醛的荧光和生物发光检测。研究表明,这两种基因编码的探针均能在缓冲溶液和活细胞中检测生理浓度相关的甲醛,并在活细胞中对甲醛进行可视化成像检测。利用基因编码的甲醛荧光探针,研究人员进一步证实了在叶酸衍生物的代谢循环中可产生内源甲醛。这项工作为研究和揭示内源甲醛的生理和病理功能提供了新的化学生物学工具,同时为发展基于活性的传感策略提供了新的思路。
相关工作发表在《德国应用化学》期刊上(Angewandte Chemie International Edition, DOI: 10.1002/anie.202001425),我院彭涛老师为唯一通讯作者,彭涛课题组博士研究生张雨晴和杜一萌为共同第一作者。彭涛课题组博士研究生李曼佳和张栋也参与了该研究,我院项征老师提供了质粒上的帮助。该工作得到了国家自然科学基金委和深圳市科技创新委员会的基金支持。
论文链接:https://onlinelibrary.wiley.com/doi/10.1002/anie.202001425