近日,北京大学深圳研究生院/深圳湾实验室黄昊团队在《Cell Death & Disease》上发表了题为“ISGylation prevents autophagic degradation of STING and promotes antitumor immunity in lung cancer”的研究论文[1]。该研究揭示了ISGylation修饰在稳定STING蛋白、增强抗肿瘤免疫中的关键作用,并鉴定出一种潜在的抗肿瘤药物候选分子,为肺癌免疫治疗提供了新策略。
1. ISGylation稳定STING并阻断其自噬降解
STING通路在介导抗肿瘤免疫中发挥核心作用,然而在包括肺癌在内的多种癌症中,STING蛋白水平的下降常导致免疫治疗效果受限。黄昊团队通过深入研究发现,ISGylation(干扰素刺激基因15修饰)能够通过防止STING发生自噬降解,从而显著稳定STING蛋白水平,进而增强其免疫刺激功能。研究进一步揭示,去ISGylation酶USP18作为该过程的负调控因子,能够移除STING上的ISGylation修饰,导致STING通过降解(图1)。
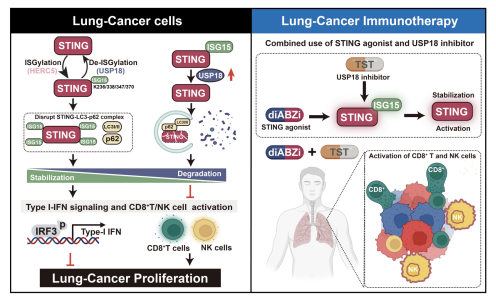
图1 STING的ISGylation阻止肺癌发生发展,以及USP18抑制剂激发抗肿瘤免疫反应
2. 靶向USP18增强抗肿瘤免疫响应
基于上述机制,研究团队鉴定出丹参酮IIA磺酸钠(TST)作为一种有效的USP18抑制剂。实验表明,TST能够通过抑制USP18活性,提升STING的ISGylation水平,从而维持STING蛋白的稳定性。更重要的是,在与STING激动剂diABZi联用时,TST展现出显著的协同效应,能够有效激发强效的抗肿瘤免疫反应。这一发现不仅阐明了STING蛋白稳态调控的分子机制,还为通过小分子抑制剂增强STING通路活性、提升肺癌免疫治疗疗效开辟了新的临床应用路径(图1)。
该文章共同第一作者为实验室前成员曹丹博士(现为斯坦福大学博士后)和黄斌博士(现为哈尔滨医科大学副教授),参与该工作的还有傅鑫铭、刘明、牛晓刚、翟宏斌等。该研究工作得到了国家自然科学基金、广东省基础与应用基础研究、深圳市科技项目及深圳湾实验室等相关基金的大力支持。
此前,课题组曾报道在病毒入侵时,STING的去泛素化修饰介导了宿主天然免疫的下调[2],并据此报道了抗病毒治疗的新策略。综上所述,黄昊课题组围绕STING的翻译后修饰,及其在人体先天免疫调控和肿瘤发生发展中的作用做出了一系列深入、系统的研究,并提出了创新性的治疗策略,为相关重大疾病的临床治疗提供了重要的理论参考。
References:
Cao D, Huang B, Fu X, Liu M, Niu X, Zhai H, Huang H., ISGylation prevents autophagic degradation of STING and promotes antitumor immunity in lung cancer. Cell Death Dis. 2026 Feb 27;17(2):8527.
Cao D, Duan L, Huang B, Xiong Y, Zhang G, Huang H., The SARS-CoV-2 papain-like protease suppresses type I interferon responses by deubiquitinating STING. Sci Signal. 2023 May 2;16(783):eadd0082.





